A cura di Susanna Ciraci
infermiera terapia intensiva neonatale fondazione poliambulanza di Brescia
La ventilazione oscillatoria ad alta frequenza (High Frequency Oscillatory Ventilation, HFOV) rappresenta una strategia ventilatoria protettiva non convenzionale ampiamente utilizzata in neonatologia. L’HFOV viene spesso utilizzata come terapia rescue con l’obiettivo di migliorare gli scambi gassosi quando la ventilazione convenzionale fallisce, ma è un valido trattamento iniziale anche in casi di sindrome da air leak, ipertensione polmonare persistente e sindrome da aspirazione di meconio [1].
HFOV è caratterizzata da frequenze sovrafisiologiche e bassi volumi correnti: la logica di tale ventilazione si sviluppa attorno alla generazione di oscillazioni ad alta frequenza su una pressione di distensione polmonare (equivalente alla pressione media delle vie aeree, MAP, meglio definita in HFOV come continuous distending pressure, CDP) tale da prevenire il dereclutamento alveolare e garantire la massimizzazione della superficie di scambio (figura 1). Attorno alla pressione di distensione polmonare, un meccanismo a pistone genera oscillazioni pressorie a frequenze comprese tra 180 e 1200 oscillazioni al minuto (3-20 Hz) che determinano l’erogazione di volumi correnti particolarmente bassi [2].
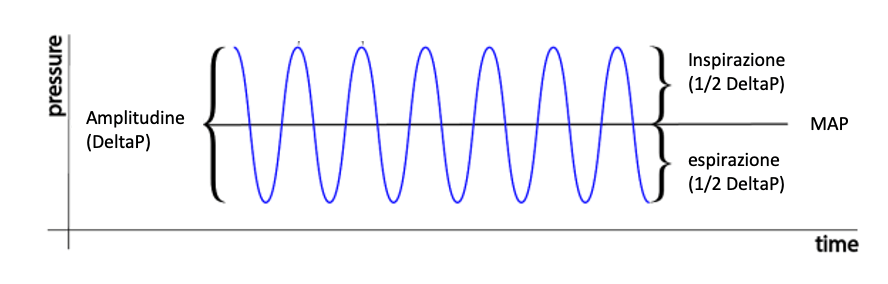
Particolarità tipica di tale ventilazione, che la rende protettiva nei confronti del polmone immaturo del neonato, è proprio l’erogazione di bassi volumi correnti, per definizione inferiori allo spazio morto anatomico, che in neonatologia corrispondono a 1/2 – 1/3 dei volumi erogati in ventilazione convenzionale.
Le oscillazioni pressorie, inoltre, tendono ad attenuarsi progressivamente lungo l’albero respiratorio (figura 2), determinando variazioni pressorie a livello alveolare particolarmente ridotte, con conseguente riduzione del rischio di barotrauma.
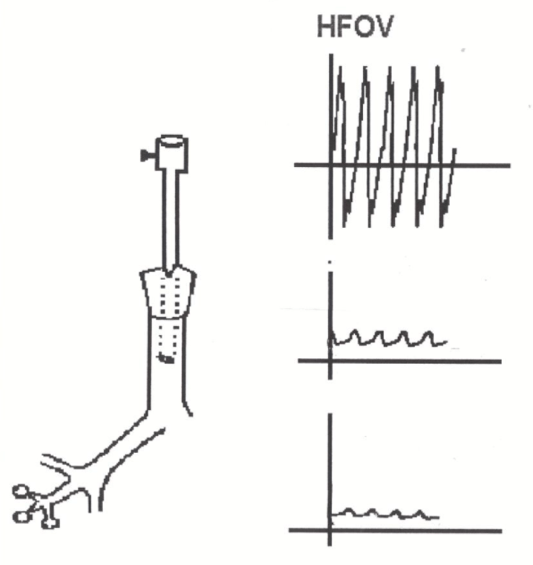
In HFOV sia l’inspirazione che l’espirazione risultano essere attive, come conseguenza del movimento del meccanismo a pistone che si sposta in avanti creando pressione positiva in fase inspiratoria, e indietro creando pressione negativa in fase espiratoria [3].
Com’è possibile ventilare con volumi correnti così ridotti?
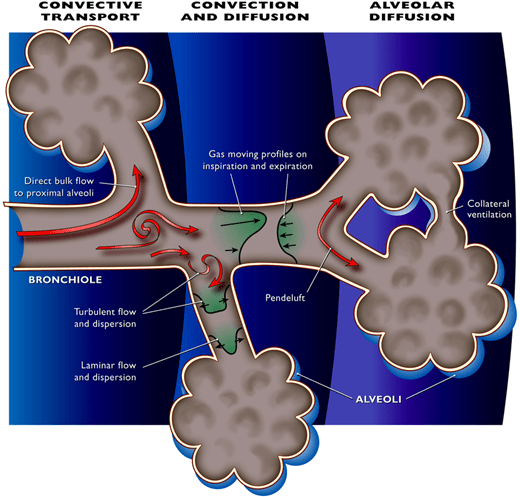
Vi sono particolari meccanismi di trasporto dei gas nell’albero respiratorio che concorrono a garantire adeguate ossigenazione ed eliminazione dell’anidride carbonica (figura 3), tra cui:
- la creazione di vortici turbolenti nelle grandi vie aeree che giocano un ruolo decisivo nel rapido trasporto di ossigeno;
- l’asimmetria dei profili di flusso inspiratori ed espiratori, grazie alla quale i gas ricchi di ossigeno risultano essere trasportati più velocemente nella porzione inferiore delle vie respiratorie, grazie ai loro profili di flusso più netti e penetranti, mentre i gas poveri di ossigeno, i cui profili di flusso risultano più smussi, vengono efficientemente trasportati verso la porzione superiore delle vie aeree;
- l’effetto Pendelluft, per il quale i gas contenuti in unità alveolari con differenti costanti di tempo si spostano verso le unità prossime al collasso [4].
Le variabili regolabili al ventilatore sono:
- CDP o MAP, che a differenza della ventilazione convenzionale è possibile impostare;
- Frequenza espressa in Hz (1Hz=60 oscillazioni/minuti);
- Amplitudine o Delta P, ovvero l’ampiezza delle oscillazioni;
- Rapporto I:E, espresso in percentuale di tempo inspiratorio su alcuni ventilatori (Sensor Medics 3100A e 3100B).
- FiO2
Una caratteristica esclusiva di questa modalità di ventilazione è il fenomeno del disaccoppiamento: la regolazione dello scambio di ossigeno e la regolazione dello scambio di anidride carbonica possono essere effettuate in maniera indipendente regolando diversi parametri, a differenza di quanto avviene in ventilazione convenzionale. La regolazione dell’ossigenazione è direttamente correlata alla modulazione della frazione inspirata di ossigeno (FiO2) ed al volume polmonare, che in HFOV dipende esclusivamente dalla CDP o MAP [2]. Al fine di migliorare l’ossigenazione, dunque, l’operatore può agire modulando la FiO2 o la MAP. La modulazione della MAP permette il reclutamento di superficie alveolare utile allo scambio gassoso, con conseguente effetto positivo sulla PaO2. La sua regolazione deve avvenire tuttavia in maniera conservativa, al fine di prevenire il fenomeno di sovradistensione [5]. Per regolare lo smaltimento della CO2 invece, è possibile agire sulla frequenza e sull’amplitudine o Delta P. L’ampiezza dell’oscillazione determina il volume corrente, dunque all’aumentare dell’amplitudine aumenterà anche il volume erogato al paziente, migliorando così lo smaltimento della CO2. Anche la modulazione della frequenza in HFOV, contrariamente a quanto avviene in ventilazione convenzionale, ha effetto diretto sullo spostamento di volumi: una frequenza minore determina un maggior volume corrente e dunque maggior eliminazione di anidride carbonica.
Sui più recenti ventilatori neonatali è stata introdotta la possibilità di settare un controllo aggiuntivo, il Volume Garantito. Come avviene in ventilazione convenzionale, anche in HFOV è possibile impostare un target di volume corrente, lasciando al ventilatore la possibilità di regolare l’amplitudine pressoria per raggiungere il volume settato, pur mantenendo un valore soglia al fine di prevenire il rischio di barotrauma. L’obiettivo di tale controllo aggiuntivo è quello di limitare il danno polmonare indotto dalle frequenti fluttuazioni di volume corrente, permettendo un mantenimento più regolare e costante nel tempo di volumi entro il range prestabilito [6].
Durante la ventilazione ad alta frequenza oscillatoria è necessario un assiduo monitoraggio del neonato, con particolare attenzione ad alcuni aspetti:
- al fine di trasmettere le oscillazioni adeguatamente e progressivamente attenuate nell’albero respiratorio, il circuito utilizzato deve essere rigido e a bassa compliance [5]. Circuito e tubo endotracheale vanno mantenuti il più possibile in asse, senza curvature marcate che interferiscano con la trasmissione delle oscillazioni;
- i flussi erogati in HFOV sono particolarmente elevati, dunque risultano di fondamentale importanza umidificazione e riscaldamento adeguati e continui dei gas, al fine di prevenire danni irreversibili alla superficie epiteliale del tratto respiratorio. L’assenza di adeguata umidificazione comporta la formazione di secrezioni dense e viscose che possono ostruire i bronchi, determinando il collasso dei compartimenti alveolari a valle. La ridotta compliance che ne deriva determina inoltre un aumento del rischio di barotrauma, secondario all’aumentata trasmissione delle oscillazioni pressorie alla periferia [7];
- un’eccessiva umificazione può arrecare danni, con accumulo di condensa nel circuito e conseguente compromissione dell’adeguata erogazione di volumi correnti;
- l’aspirazione endotracheale in HFOV rappresenta una valida misura preventiva del collasso alveolare e degli episodi di atelettasia; la presenza di secrezioni anche in scarse quantità può, infatti, interferire con l’efficacia del trattamento, aumentando le resistenze nelle vie aeree e riducendo significativamente l’erogazione di volumi correnti. Le oscillazioni pressorie, inoltre, possono favorire l’accumulo di secrezioni nelle aree distali promuovendo il trauma locale. La manovra di aspirazione nel neonato in HFOV può causare una perdita transitoria di volume, qualora venga effettuata con un sistema aperto di aspirazione [8]. L’utilizzo di circuiti chiusi di aspirazione riduce tale complicanza, prevenendo o riducendo il dereclutamento polmonare [7,9]. Tuttavia, anche con l’utilizzo dei circuiti chiusi può essere necessaria una breve manovra di reclutamento polmonare subito dopo l’aspirazione, al fine di ripristinare il volume polmonare. Tale manovra viene eseguita aumentando temporaneamente la CDP o MAP;
- in corso di HFOV è importante monitorare in maniera continua anche l’assetto cardiovascolare, poiché l’applicazione continua di una pressione di distensione polmonare può influire sull’interazione tra sistema polmonare e sistema cardiovascolare. Gli effetti cardiovascolari dell’HFOV comprendono una possibile riduzione del ritorno venoso e della portata cardiaca, con conseguente riduzione delle pressioni sistemiche [5,7].
Un caro saluto a tutti
Susanna Ciraci
Bibliografia
- Rettig JS, Smallwood CD, Walsh BK, Rimensberger PC, Bachman TE, Bollen CW, et al. High-Frequency Oscillatory Ventilation in Pediatric Acute Lung Injury: A Multicenter International Experience. Crit Care Med. dicembre 2015;43(12):2660–7.
- Raccomandazioni sulla ventilazione ad alta frequenza oscillatoria (HFOV) nel neonato – SIN Disponibile su: https://www.sin-neonatologia.it/raccomandazioni-sulla-ventilazione-ad-alta-frequenza-oscillatoria-hfov-nel-neonato/
- Bouchut J-C, Godard J, Claris O. High-frequency oscillatory ventilation. Anesthesiology. aprile 2004;100(4):1007–12.
- Roth CJ, Förster KM, Hilgendorff A, Ertl-Wagner B, Wall WA, Flemmer AW. Gas exchange mechanisms in preterm infants on HFOV – a computational approach. Sci Rep. 29 agosto 2018;8(1):13008.
- Meyers M, Rodrigues N, Ari A. High-frequency oscillatory ventilation: A narrative review. Can J Respir Ther CJRT Rev Can Thérapie Respir RCTR. 2 maggio 2019;55:40–6.
- Iscan B, Duman N, Tuzun F, Kumral A, Ozkan H. Impact of Volume Guarantee on High-Frequency Oscillatory Ventilation in Preterm Infants: A Randomized Crossover Clinical Trial. Neonatology. 2015;108(4):277–82.
- Jane Pillow. High Frequency Oscillatory Ventilation: Theory and Practical Application. Drägerwerk AG & Co. KGaA, Germany; 2016.
- Tingay DG, Copnell B, Mills JF, Morley CJ, Dargaville PA. Effects of open endotracheal suction on lung volume in infants receiving HFOV. Intensive Care Med. 1 aprile 2007;33(4):689–93.
- Kiraly NJ, Tingay DG, Mills JF, Morley CJ, Dargaville PA, Copnell B. The effects of closed endotracheal suction on ventilation during conventional and high-frequency oscillatory ventilation. Pediatr Res. ottobre 2009;66(4):400–4.