A cura di Alice Galesi
Nella prima parte dell’articolo, (clicca qui per il rimando alla parte 1), sono stati descritti i sistemi di nebulizzazione. Oggi, si presentano i fattori relativi al ventilatore e al circuito del ventilatore per capire come questi influenzano l’erogazione di aerosol durante la ventilazione meccanica.
Fattori relativi al ventilatore
Le impostazioni del ventilatore influiscono sull’erogazione del farmaco [1]: un tidal volume di 500 ml o più (in un adulto), un tempo inspiratorio più lungo e flussi inspiratori più lenti migliorano l’erogazione di aerosol [1,5]. Flussi inspiratori da 30 a 50 L/min sono ottimali per la somministrazione dei farmaci per via inalatoria. Tuttavia, flussi inspiratori più lenti possono incrementare il tempo inspiratorio con conseguente riduzione di quello espiratorio, provocando un potenziale aumento della pressione positiva di fine espirazione [1]. La dose farmacologica è direttamente proporzionale ad un ciclo respiratorio più lungo sia per gli inalatori pressurizzati predosati (pMDI), che per i nebulizzatori [1]. Il meccanismo di attivazione del respiro o trigger inspiratorio non influenza significativamente la somministrazione di farmaci erogati attraverso un pMDI, ma l’uso di un trigger a flusso con un nebulizzatore potrebbe diluire l’aerosol e aumentare il washout del farmaco [1].
Sincronizzazione della generazione di aerosol con il ciclo respiratorio
Con i pMDI, è necessario coordinare l’erogazione di aerosol con l’inizio dell’inspirazione [5]. Con un Jet Nebulizer (JN) o nebulizzatore pneumatico a getto, la sincronizzazione può essere ‘continua’, ‘intermittente sulla fase inspiratoria’ o ‘intermittente sulla fase espiratoria’, grazie a diversi modelli di ventilatori, che forniscono opzioni variabili. Da uno studio di confronto sulle tre diverse modalità di erogazione è emerso che le dosi di farmaco erogate erano simili [2]. Anche il dispositivo vibrating mesh nebulizer (VMN) o nebulizzatore a membrana vibrante, qualora il ventilatore ne garantisse l’opzione, può funzionare in modo continuo o intermittente.
Fattori relativi al circuito del ventilatore
Dopo l’inserimento di un tubo endotracheale (ETT) o tracheostomico (TT), muco e biofilm possono accumularsi sulla superficie del presidio, creando superfici irregolari e restringendo il diametro delle vie aeree artificiali. Il diametro stretto del ETT e del TT rispetto alle normali vie aeree, in combinazione con gli elevati flussi inspiratori impiegati durante la ventilazione meccanica alterano l’erogazione di aerosol [2]. Pertanto, se la dose di farmaco viene alterata per le dimensioni e la lunghezza delle vie aeree artificiali, si devono considerare dosaggi diversi per ottenere una risposta clinica efficace [2].
Calore, umidificazione e densità dei gas inalati
Per prevenire danni alla mucosa delle vie aeree, si utilizzano due strategie per riscaldare e umidificare i gas secchi erogati in ingresso dai ventilatori: l’umidificazione attiva e lo scambiatore di umidità e calore (HME). Gli umidificatori attivi riscaldano una massa d’acqua, che entra a contatto con il gas freddo mentre si sposta nel circuito del ventilatore verso il paziente, con l’obiettivo di fornire un’umidità relativa >90% a 35–37 °C [2]. Al contrario, il materiale igroscopico/idrofobico del filtro HME cattura il calore e l’umidità dal gas espirato dal paziente e restituisce fino al 70% di entrambi al gas erogato al paziente durante l’inspirazione successiva [2]. Diversi studi hanno dimostrato che la dose di farmaco in aerosol, somministrata sia dai pMDI che dai nebulizzatori, è ridotta fino al 50% in un circuito umidificato rispetto ad uno secco [1,2]. L’umidità del circuito aumenta le dimensioni delle particelle di farmaco generate da un nebulizzatore [1]; mentre quando è in uso un pMDI, l’umidità probabilmente interferisce con l’evaporazione del propellente in modo che le particelle di farmaco rimangono di dimensioni maggiori e le perdite da impatto inerziale aumentano [1]. È possibile superare l’effetto dell’umidificazione spegnendo l’umidificatore durante l’erogazione dell’aerosol [2]. Tuttavia, nello studio di Lin e colleghi è stato dimostrato che lo spegnimento dell’umidificatore fino a 40 minuti prima della somministrazione di pMDI non aumentava l’erogazione dell’aerosol [6]. Nello studio di Moustafa et al [7], trentasei pazienti ventilati meccanicamente hanno ricevuto il broncodilatatore attraverso tre generatori di aerosol, con o senza umidificazione. Sono stati confrontati i livelli farmacologici di salbutamolo urinario e hanno rivelato che l’umidità non influenza la biodisponibilità con nessuno dei dispositivi testati [7]. Hanno inoltre determinato l’influenza dell’umidità sulla risposta clinica, considerando la durata dell’ospedalizzazione e della ventilazione meccanica, e hanno riferito che la somministrazione di aerosol con o senza umidificazione non ha avuto effetti significativi su tali esiti clinici [7]. Pertanto, si consiglia di non interrompere l’umidificazione attiva durante la somministrazione di aerosol [2].
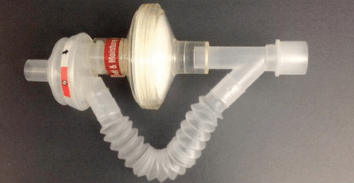
Gli HME devono essere rimossi durante la somministrazione dell’aerosol, perché da un lato catturano le particelle di farmaco, riducendo notevolmente l’efficienza della somministrazione (se posizionati tra nebulizzatore e paziente) [1,2], dall’altro potrebbero ostruirsi aumentando in modo esponenziale le resistenze al flusso delle vie aeree. Ci sono HME noti per essere permeabili all’aerosol (Fig 1), che non vengono rimossi dal circuito ma riducono la dose inalata fino al 40%; di conseguenza la dose di farmaco dovrà essere aggiustata [2]. Invece, alcuni HME sono stati riprogettati per reindirizzare l’aerosol dal circuito del ventilatore alla parte distale di un TET durante la terapia inalatoria (Fig 2)[2].


Anche la densità del gas inalato influenza la somministrazione di farmaci. Elevati flussi inspiratori impiegati durante la ventilazione sono associati a turbolenza. L’inalazione di un gas meno denso, come una miscela elio-ossigeno, rende il flusso d’aria meno turbolento e più laminare [1] rendendo la somministrazione più efficacie. Prima di impiegare elio-ossigeno in pazienti ventilati, è importante assicurarsi che il ventilatore sia compatibile con l’uso di tali miscele di gas [1].
Posizione dei nebulizzatori e dei pMDI nel circuito
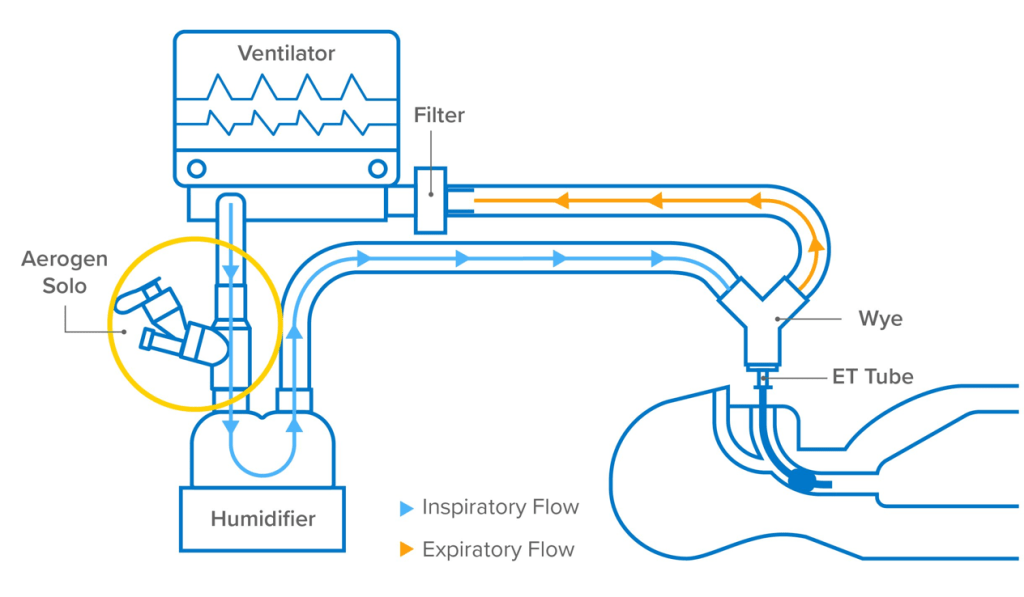
Con i pMDI, per ottenere la massima efficacia, bisogna erogare il farmaco vicino al tubo endotracheale (raccordo a Y) [2]. Mentre, con il nebulizzatore a getto e a membrana vibrante, si riporta una dose maggiore di farmaco quando posti vicino al ventilatore; il motivo è perché questi sistemi possono erogare farmaco in continuo (sia in fase inspiratoria che espiratoria) [1,2]. Gli autori hanno ipotizzato che l’aerosol erogato in continuo, lontano dal paziente, possa essere trattenuto dalla branca inspiratoria, come un serbatoio, durante la fase espiratoria [2]. La terapia inalatoria, è tuttavia influenzata dal tipo di trigger inspiratorio. Il trigger a flusso è progettato con il passaggio di un flusso continuo di gas o bias flow tra la valvola inspiratoria ed espiratoria. Pertanto, il bias flow è un elemento che influenza la somministrazione dei farmaci aerosol [2]. Con 2 e 5 L/min di bias flow, VMN e JN risultano a maggior ragione più efficienti se posizionati vicino al ventilatore e non prossimali al paziente (raccordo a Y) [2], dove la dose di farmaco viene veicolata più facilmente verso la branca espiratoria [2]. Si ricorda che il nebulizzatore a membrana vibrante è il sistema più efficiente in termini di maggior dose di farmaco erogata [2]. I sistemi Aerogen Pro o Solo, sono esempi di nebulizzatori mesh progettati per essere compatibili con i circuiti del ventilatore meccanico. Nel manuale d’uso del sistema Aerogen Solo è indicato il posizionamento sul lato secco dell’umidificatore (Fig 3), quindi all’ingresso dell’umidificatore [9]. Tuttavia, Anderoson e colleghi hanno notato che non ci sono differenze sull’efficacia del farmaco erogato, posizionando VMN all’entrata o all’uscita dell’umidificatore [6].
Uso di un filtro HEPA prima del flussometro espiratorio
Durante la nebulizzazione, una quantità significativa di goccioline viene eliminata attraverso l’arto espiratorio del circuito del ventilatore [5]. Le goccioline possono danneggiare il misuratore di flusso espiratorio del ventilatore (qualora fosse integrato nella macchina)*, è consigliabile proteggerlo posizionando un filtro sull’arto espiratorio (prima del flussometro) [5]. Le particelle espirate hanno un impatto sul filtro protettivo, causando un aumento della resistenza espiratoria. Se l’ostruzione diventa completa le conseguenze sono potenzialmente gravi (aumento della pressione positiva di fine espirazione e aumento del lavoro respiratorio). Pertanto, per la sicurezza del malato, il filtro va regolarmente cambiato ad ogni ciclo della terapia inalatoria [5].
*Sono disponibili in commercio ventilatori con flussometri espiratori esterni non integrati nel circuito
Costo-efficacia della terapia
Le tecniche ottimali, per somministrare la terapia inalatoria nei pazienti ventilati, si basano sui fattori discussi sopra. Una buona tecnica potrebbe essere il compromesso tra le caratteristiche operative del dispositivo e le condizioni del paziente [1]. La scelta del dispositivo deve considerare il costo del nebulizzatore, il costo del farmaco, la dose da erogare e il tempo del trattamento terapeutico [2]. Dallo studio di Liu e colleghi emerge che il costo totale, per una settimana di trattamento con colistina con un VMN è inferiore a quello con JN, anche se un VMN è più costoso di un JN. Quindi, è importante saper bilanciare disponibilità e costi per identificare l’aerosolterapia più conveniente nel contesto clinico specifico [2].
Riassumendo
- Diminuire il flusso inspiratorio, aumentare il tempo inspiratorio e/o il tidal volume.
- Se si utilizza un umidificatore riscaldato, non spegnere o scollegare prima o durante il trattamento.
- Rimuovere HME tra il generatore di aerosol e il paziente o utilizzare HME noto per essere permeabile all’aerosol.
- Rimuovere il filtro HEPA al termine dell’aerosol e cambiarlo ad ogni ciclo della terapia inalatoria.
- Posizione dispositivo: pMDI sulla linea inspiratoria (raccordo a Y); JN e VMN sul lato secco o all’uscita dall’umidificatore.
- Per pMDI: agitare e innescare prima dell’uso, collegare al distanziatore o all’adattatore; attuare all’inizio dell’ispirazione. Attendere 30-60 secondi tra un’attuazione e l’altra. Rimuovere il contenitore.
- Per il nebulizzatore a getto: utilizzare la fonte di gas sul ventilatore per sincronizzare la nebulizzazione con l’ispirazione, se disponibile; in caso contrario, impostare il gas da 6 a 10 L/min come raccomandato sull’etichetta del nebulizzatore per la nebulizzazione continua e regolare i limiti di volume o pressione del ventilatore e allarmi per compensare il flusso e il volume aggiunti al circuito durante la somministrazione di aerosol [2].
- Dopo l’uso: rimuovere JN dal circuito (poiché il contenitore di farmaco è aperto e lasciato in sede causa perdite aeree dal circuito); lasciare in sede VMN (il cui contenitore è chiuso) secondo le indicazioni del produttore
Un caro saluto a tutti
Alice Galesi
Blibliografia
- Tobin MJ. Principles and practice of mechanical ventilation. New York: McGraw Hill; 2013.
- Hui-Ling L, Fink JB, Huiqing G. Aerosol delivery via invasive ventilation: a narrative review. Ann Transl Med, 2021; 9(7):588.
- Arzu A, Atalay OT, Harwood R, et al. Influence of nebulizer type, position, and bias flow on aerosol drug delivery in simulated pediatric and adult lung models during mechanical ventilation. Respir Care,2010;55(7):845-51.
- Miller D, Amin M, Palmer LB, et al. Aerosol delivery and modern mechanical ventilation: in vitro/in vivo evaluation. Am J Respir Crit Care Med, 2003;168:1205-9.
- Ehrmann S, Roche-Campo F, Sferrazza GF, et al. Aerosol therapy during mechanical ventilation: an international survey For the REVA research network. Intensive Care Med, 2013; 39(6):1048-56.
- Anderson AC, Dubosky MN, Fiorino KA, et all. The Effect of Nebulizer Position on Aerosolized Epoprostenol Delivery in an Adult Lung Model.
- Moustafa IOF, ElHansy MHE, Al Hallag M, et al. Clinical outcome associated with the use of different inhalation method with and without humidification in asthmatic mechanically ventilated patients. Pulm Pharmacol Ther 2017;45:40-6.
- Berlinski A, Willis JR. Effect of tidal volume and nebulizer type and position on albuterol delivery in a pediatric model of mechanical ventilation. Respir Care 2015;60:1424-30.
- Sito: 30-674-Rev-G-Aerogen-Solo-System-IM-US-WEB.pdf
- Sito: A Lung Recruitment Strategy for Patients with Respiratory Failure utilising Aerogen (microbiozhealth.com)
- Arzu A. Aerosol therapy in pulmonary critical care. Respir Care, 2015;60:858-874.